Le plasma est obtenu, soit à partir de don du sang après centrifugation et séparation des différents constituants du sang, soit lors d'un don d'aphérèse (plasmaphérèse). Le plasma est utilisé pour la transfusion de malades et la fabrication des médicaments dérivés du sang. Ces médicaments dérivés du sang (facteurs de coagulation, Albumine, Immunoglobulines) sont fabriqués en France, par le Laboratoire de Fractionnement et des Biotechnologies (LFB).
La plasmaphérèse est réalisée par un automate qui prélève le plasma issu du sang du donneur et réinjecte les autres constituants du sang (plaquettes, globules blancs et globules rouges). Les plasmas ainsi prélevés sont déjà déleucocytés. Ils doivent avoir un volume d'au moins 200 mL et une concentration en facteur VIII supérieure à 0,7 UI/mL.
Le plasma n'est jamais irradié, en raison de la faible quantité de cellules immuno-compétentes et des opérations de congélation-décongélation qui altèrent ces cellules.
En plus des analyses réalisées sur les donneurs de sang par le service de qualification biologique des dons (QBD), le plasma bénéficie d'une sécurisation systématique vis-à-vis des risques de transmission d'agents infectieux (sécurisation par quarantaine, par viro-atténuation ou inactivation d'agents pathogènes).
Sécurisation par quarantaine
Le Plasma Frais Congelé Sécurisé (PFC-Se) par quarantaine ne subit aucun traitement. La sécurisation consiste à mettre en quarantaine les plasmas congelés durant une période minimale de 60 jours. Le plasma est libéré à la suite d'analyses supplémentaires réalisées chez le donneur de sang lors d'un second don. Ce type de sécurisation oblige donc le donneur à revenir pour un prélèvement supplémentaire afin de réaliser sa sérologie, 60 jours après son don. Les unités de plasma sont comprises entre 200 mL et 850 mL.
Viro atténuation d'agents pathogènes par solvant-détergent
Depuis 2015, le Plasma Frais Congelé viro-atténué par Solvant Détergent (PFC-SD) est devenu un médicament dérivé du sang et n'est plus fabriqué en France. Ce plasma est fabriqué par des entreprises pharmaceutiques étrangères. Il est obtenu à partir d'un mélange de plasmas de 400 à 1500 donneurs de même groupe sanguin ABO.
L'inactivation des agents pathogènes débute lors de la congélation et décongélation du plasma qui conduit à la destruction des cellules, puis par l'action d'un solvant (tri n-butyl phosphate : TnBP) et un détergent (Triton X100) à 30°C pendant 4 heures. Après traitement physique et chimique, le plasma nécessite plusieurs filtrations afin d'éliminer la totalité des cellules (donc des pathogènes intracellulaires), des débris cellulaires (donc des antigènes plaquettaires, érythrocytaires, leucocytaires) et des bactéries. Le solvant et le détergent sont éliminés par l'huile de ricin et par chromatographie. Ensuite, le plasma est réparti en unités de 200 mL, puis congelé. Ce traitement est efficace vis à vis des virus à enveloppe lipido-proteïque (HIV, HTLV, HBV, HCV). De plus, le mélange des donneurs a l'avantage de diluer les éventuels anticorps HLA contenus dans les plasmas et conduisant à un TRALI.
Inactivation d'agents pathogènes par amotosalen
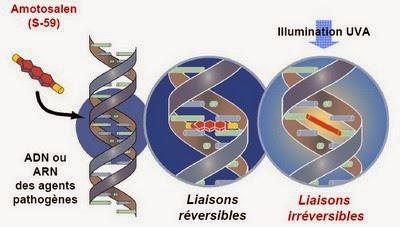
Le Plasma Frais Congelé Inactivé par Amotosalen (PFC-IA) est réalisé à partir d'un plasma unitaire déleucocyté, puis traité par un psoralène (amotosalen-HCI). Le plasma est mis en contact avec une solution d'amotosalen-HCI puis illuminé par les ultraviolets A (UVA).
L'amotosalen HCI s'intercale de façon réversible entre les régions héllicoïdales de l'ADN et de l'ARN. L'illumination par les UVA de 320 à 400 nm conduit à la formation de liaisons covalentes avec les bases pyrimidiques des acides nucléiques. Les génomes ainsi réticulés des agents pathogènes et des leucocytes ne peuvent plus fonctionner ni se répliquer.
L'amotosalen résiduel est éliminé par une adsorption spécifique. Ces unités sont comprises entre 200 et 300 mL. L'inactivation par amotosalen est efficace sur les virus nus et enveloppés, les bactéries, les parasites et les leucocytes. Elle est contre-indiquée chez les patients ayant une allergie à l'amotosalen.
Plasma lyophilisé
Le plasma lyophilisé est préparé à partir de plasma frais congelé traité par l'amotosalen provenant de 10 donneurs. Ces plasmas sont ensuite lyophilisés afin de faire du plasma A, B ou AB sous forme de poudre. Ce plasma lyophilisé est reconstitué avant la transfusion avec de l'eau PPI fournie dans le coffret de distribution. Ce produit est fabriqué en France par le Centre de Transfusion Sanguine des Armées (CTSA).